
3月13日,国家药监局(NMPA)正式批准了超目科技“i-NYS植入式眼部肌肉神经刺激器”上市,先送上一波祝贺。这张国内首创、甚至是全球首创的三类有源植入医疗器械注册证,出现的时间节点有些微妙。
就在同一天,博睿康的重大进展将国内侵入式脑机接口产业的热度推向了顶点。资本市场的狂欢与媒体的聚光灯,几乎全部倾注在了这枚直接贴附于大脑皮层的电极上。
在脑机接口宏大叙事的掩盖下,超目科技这款针对眼部外周神经的植入式设备,并未能在泛科技舆论场中激起与其技术分量相匹配的水花。

但仔细研究后发现,i-NYS的获批,其背后的产业穿透力不亚于任何一款中枢神经脑机接口系统的落地。
我们需要先厘清i-NYS在临床上解决的确切痛点。先天性眼球震颤(CN)长期以来被眼科学界视为“不治之症”,其核心表现为眼球不自主的节律性摆动,导致患者终身伴随严重的视力下降和双眼视功能障碍。在此之前,临床上缺乏能够从底层神经机制上干预该疾病的有效手段。
i-NYS的破局之处在于,它将神经电刺激技术降维应用到了眼外肌的精准调控上。从已公布的71例多中心临床试验数据来看,其术后6个月的黄斑中心凹注视时间(FP)提升了587%,震颤幅度和频率分别下降了80%左右。这是一次从0到1的实质性跨越,用工程化的硬件手段,强行拉停了失控的生理节律。
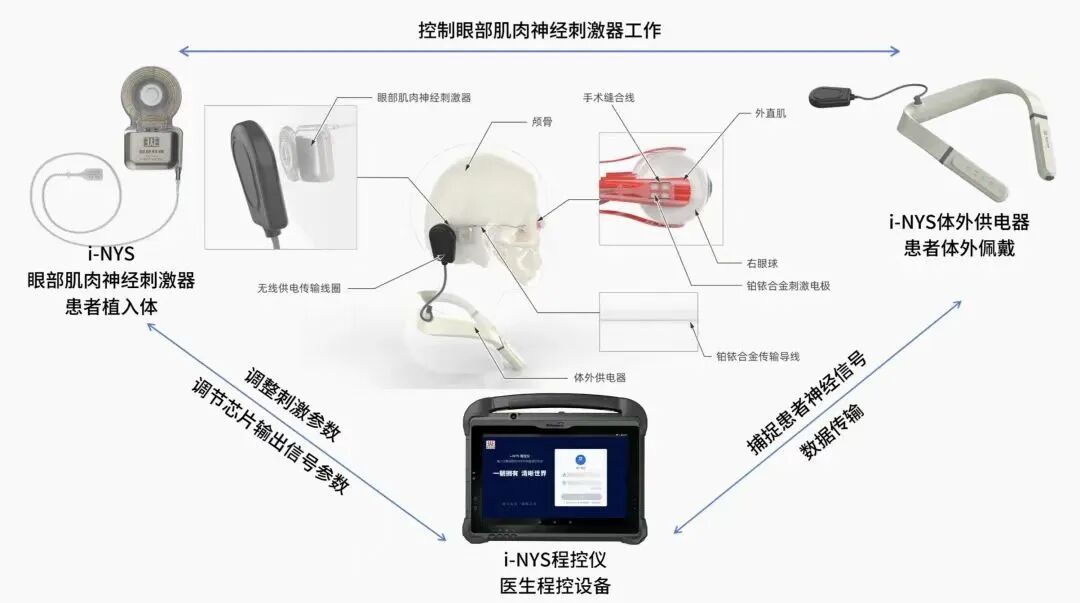
从严格的神经科学定义来看,i-NYS属于神经调控领域下的外周神经刺激器(PNS)。它并不直接与中枢神经系统(大脑或脊髓)对话,也不涉及大脑皮层意图的高级解码与编码,本质上是一个高度精密的电刺激执行器。

*图源:超目科技公众号
i-NYS能够成功拿下NMPA的三类有源植入医疗器械证,并获得美国FDA的HUD认定,意味着超目科技在几个核心的供应链节点上完成了彻底的闭环:低功耗神经刺激专用芯片(ASIC)的自主流片与系统集成、微型电极的加工制造、以及最艰难的三类植入物级高分子材料的生物相容性封装与长期气密性测试。
超目科技以眼部肌肉神经调控为切入点,完成从底层芯片到终端器械再到临床转化的全链条打通,但这显然只是其宏大战略的冰山一角。
事实上,i-NYS 的成功获批,更像是超目科技在向更深水区进发前的一场完美“实弹演习”。 官方信息显示,基于这套已经跑通中美双重认证的底层软硬件底座,超目科技正在全面推进“视觉重建”脑机接口技术的研发。
从调控外周眼外肌的电刺激,跨越到向中枢视觉皮层直接“写入”信号,技术维度的跨越固然巨大。但对于超目科技而言,最艰难的植入式微电子工程化泥沼、长效生物相容性考验以及极为严苛的三类医疗器械合规壁垒,已经真刀真枪地趟过了一遍。
这种在真实医疗场景中跑通的植入式硬件平台与供应链经验,正是向更复杂的“视觉重建”等脑机接口技术演进的最坚实底座。潮水退去后的产业竞争,拼的终究是谁能在植入式微电子的工程化泥沼中,稳稳地走通量产与合规的每一步。

企业背景
超目科技成立于2018年,是一家布局全球的高端眼科医疗器械和医用芯片研发企业,总部位于北京,在中美两地设有研发中心,并建有符合标准的GMP生产基地。自创立以来,公司始终坚持以自主创新为驱动,积极推动国产高端医疗器械的研发与临床转化,为全球视障患者提供新的解决方案。



![[NSR] 脑-机接口新方案!利用侧脑室植入实现稳定植入与记忆引导解码](https://xtechcon-static.oss-cn-chengdu.aliyuncs.com/xtimes/xtimes/images/2026-02-14/69903e89b4d15.jpeg)






