

百亿美金涌入,AI制药“GPT时刻”来了。


AI制药,临界点终于来了。
今年中国创新药出海交易火热,其中,AI制药公司正成为一股不容小觑的力量。2025年3月至8月期间,元思生肽、华深智药海外子公司、晶泰科技等接连完成总金额数十亿美金的BD交易。
其中,元思、华深成立仅四五年时间,便在跨国药企严格的BD挑选中取得成绩,正是通过AI改写了大分子药物研发范式、提高了研发成功率。这些交易也给予了资本市场以信心,时隔三四年,数家AI制药公司近期重新拿到了融资。
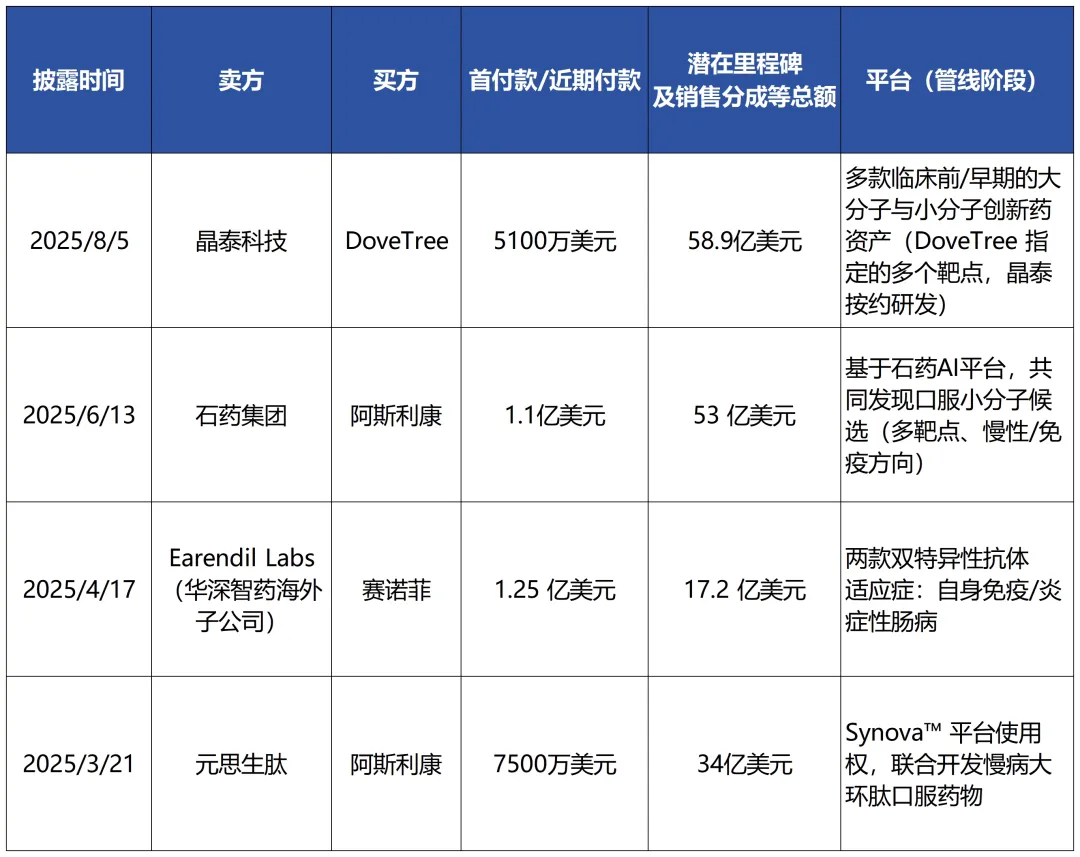
2025年部分AI制药公司BD交易
生物医药的底层研发范式,正从此前的海量筛选、经验至上,转向理性设计、从头创造。
如果说上一个十年,让早期药物发现更快、更准的AI,是“锦上添花”;那如今具备“从头设计”(de novo design)药物能力的AI,可以说是“无中生有”。而设计出自然界中不存在的蛋白质、针对难成药靶点进行药物设计,正是攻克顽疾的密码。
最近,看到Chai Discovery(openAI投资)、字节跳动等发布的蛋白质设计生成模型数据后,智源深澜创始人王承志认为“质的飞跃”就要到了。他在生命科学领域从业二十多年,曾任镁伽科技首席科学家,“放在去年,我不会下这样的判断;但今年AI的能力,让我意识到生物医药领域可能很快会有颠覆性事件发生,快到让大家没有太多思想准备。”
峰瑞资本合伙人马睿也给出了相似的判断,“现在的势能是‘创新药乘以AI’,虽然业内对AI制药的能力边界还没有定论,但我感觉已经波涛汹涌,未来一到三年应该会有翻天覆地的变化。”上一波浪潮中,A轮领投晶泰科技、天使轮领投剂泰医药,给他所在的机构带去了巨额回报,退出晶泰科技的现金回报倍数(DPI)可达几十倍。
那么,生成式AI到底如何改写新药研发底层逻辑,可能对创新药产业带来怎样的改变,当前从业者们正从哪些路径逼近“颠覆式创新”?

AI让制药
从“大海捞针”到“精准设计”
“AI制药”的故事,并非没有经历过泡沫。2018-2021年间,以小分子药物开发为代表的AI热潮,曾吸金几百亿,却未能兑现最初的愿景。当时,深度学习和虚拟筛选的路径下,AI可以加速早期药物发现进程,但筛选出的分子在效力上难以超越现有药物,或生成的全新分子结构难以合成。这本质上是早期模型“归纳能力”的局限。
新一波的AI浪潮,是主流AGI技术取得巨大进步后,能力外溢至药物研发、酶设计等生命科学领域。
首先是AlphaFold 2的出现,它验证了Transformer架构在理解“生命语言”方面同样有效,解决了困扰生物学界多年的蛋白质折叠问题。在AF2出现之前的60年,人类大概学习了20万个蛋白质的结构,但AF2出现后的两年间,AI已预测了超过2亿个蛋白质的结构,几乎涵盖地球上所有已知生命体的多数蛋白质,且高度可信。
其次,David Baker团队将图像生成领域的Diffusion(扩散)模型引入生物学,利用“迭代去噪”原理,令全新蛋白质设计的成功率,有了数量级的飞跃。
同时,AlphaFold 3从只能预测单个蛋白质结构,演进到能够处理蛋白质、核酸和小分子之间复杂的相互作用。这种“全原子级”的建模方式,让它在数据不够充分的情况下,具有更强的泛化能力。
当前,国内外有多个团队正复现并提升AF3的模型预测能力。今年年中,Chai Discovery发布的Chai-2、Evolutionary Scale发布的ESM3、字节跳动公布的Protenix等新模型的涌现,验证了”从头开始,生成全新功能分子“的创造力。
“Chai-2最新公布的数据显示,针对特定靶点,其生成的候选抗体,命中率显著高于传统方法。过去,在百万级到亿级的库里,才能筛出几个阳性分子,现在几十条序列里就可能出现hits。在以前想都不敢想。”王承志告诉36氪,这意味着,“指定靶点表位,生成抗体”的难题,正接近被解决。
传统的抗体药物研发,从确定靶点、免疫动物到筛选出有高亲和力的有效抗体,是一个漫长的“大海捞针”过程。过去可能要花费3年时间、500万美元才能解决的抗体分子发现问题,Chai-2等AI模型可以在几小时内完成,并在两周内通过生物湿实验得到验证。
马睿也表达了相似的观点,Chai Discovery可能会颠覆抗体药的研发范式,此前杂交瘤技术、噬菌体展示及动物免疫等方法,或被从头(de novo)计算设计大面积取代。如果AI在小分子设计上也能有突破性进展,那“几乎所有药物modality都可能被AI赋能。”他直言:一切发生得太快了,以至于真正看到这个图景的人还不多。
到时,药化学家要针对某个靶点设计抗体药时,第一反应可能不再是去免疫动物,而是先用AI模型进行计算、生成、打分,挑选出最有潜力的几十个抗体序列,合成并进行体外实验验证。
这种药物研发范式的改变,将对创新药产业链条带来深刻改变。
如今创新药低垂的果实已被摘完,那些因为缺乏苗头化合物,而无法被推进的“难成药”靶点研发,有望靠AI重新激活。从曾经的“有什么筛什么”,到AI时代的“要什么造什么”,人类有可能攻克一些无药可用的顽疾,一些副作用极大的药物,也可能被涌现出的更好分子取代。
王承志认为,AI将大幅缩短临床前药物研发的周期,对肿瘤、自免、代谢等领域适应症都有利好。其中,最早见到曙光的可能是“慢性病”,未来像司美格鲁肽这样百年一遇的“神药”,出现的频次会大大提高。反过来,由于AI等计算工具的推广,传统的、依赖大规模动物模型的药物筛选平台,商业价值会受到一定冲击。
未来,具有AI能力的biotech会成为跨国药企的“分子设计中心”、“算力中心”,负责前端高技术密度、高频次的药物发现;跨国药企则更多负责后期临床试验、注册准入和商业化。双方会通过管线BD授权、合作研发等模式,共分蛋糕。

钱有限,先干啥?
历次技术革命,都会带来行业洗牌,各方都在预测、选择赢面最大的玩家。临界点将至,通往未来的路径并不只有一条。如今,AI制药领域的参与者,大致呈现出三种形态。
第一类,拥有充足资本、算力的科技巨头,如Google(Deepmind)、Meta、Xaira(种子轮融资10亿美元)、字节跳动等。它们致力于打造基础生物大模型,创建自己的开源生态、定义行业标准。
第二类,顶尖AI大模型+生物计算科学家领衔的创业团队,他们有能力在算法的“无人区”进行探索。对基础模型进行优化改造后,为药企、生物科技公司提供平台服务,或自研管线。典型如百图生科、华深智药、英汐智能、分子之心、百奥几何等。
第三类,利用AI研发新药的“传统正规军”。他们不追求自研一个新的基础模型,而是根据自身对适应症、靶点、管线竞争的洞察,用AI开源模型和强大的湿实验能力,来加速特定疾病药物的研发进程。
在马睿来看,评估AI制药赛道玩家的核心竞争力,应该是其对模型的理解、修改及演进能力。从很多人利用AF3等开源模型做benchmark的结果来看,依赖微调的开源模型或许可以做到“80分”,但要解决真实研发中的复杂问题,往往需要接近“99分”的表现,只有在算法层面做到极致,才可能实现跨越式进步。
另一位生命科学领域专家则指出,绝大部分公司无法负担自研基础生物模型的高昂成本,与大语言模型相比,生物模型所依赖的数据获取成本更高。他提到,国内曾有一家巨头支持的企业,投入数千万元,合成并测试了上万条AI生成的抗体序列,并将实验数据集用于模型训练。但最终发现,这样的数据规模,仍远不足以进入scaling law所描述的高效提升区间。
王承志给出了相似观点,他认为未来能够快速、海量产出高质量生物实验数据的团队,更有可能拥有高性能AI模型。“过去,自动化、高通量实验,往往被理解为提高筛选效率。但在AI时代,它们不仅能为研发人员提供实验结果,还可以高效产生结构化、可迭代数据,直接服务于模型训练与优化。”
算法、数据,都是AI制药能力提升的核心要素。尽管各家创始人背景、团队优势不同,短期资源投入的侧重有一定差异,但AI在制药领域的产业化路径愈发接近。即研发出真正有价值的药物分子,并在当前成熟的BD体系里,获得买方认可、拿到真金白银。
“按当前趋势下,未来所有新药研发公司都会用AI,只是依赖程度不同;对AI制药公司来说,只强调模型也不行,最后还是要交付药物分子,才能被赋予更高价值。”马睿总结道,”所以我最近一直在讲:创新药就是AI制药,AI制药就是创新药。”



















