在当前的临床实践与前沿探索中,如何平衡脑电信号的采集质量与手术创伤,始终是整个行业面临的核心技术挑战之一。今天我们为大家梳理了一篇近期发表在《Journal of NeuroInterventional Surgery》上的综述文献,该文跳出了单纯的电生理信号处理视角,以神经介入医生的现实临床视角,系统性地盘点了血管内神经接口的技术演进,并深度剖析了以Synchron的Stentrode系统和Epsilon的EP-01平台为代表的现阶段前沿设备的临床转化准备情况。
作为专注脑机接口产业化落地与供应链整合的服务平台,我们希望借由这篇文献的核心框架,帮助产业链上下游的从业者更客观地认识到:血管内脑机接口要真正走向常规临床,除了攻克神经信号解析的难关之外,血管植入物的长期安全性、科学的抗血栓策略制定,以及确立具有切实临床指导意义的评价终点,同样是决定这一技术流派商业化成败的关键深水区。
转发本推文到朋友圈可以找编辑领取原文献
神经记录与刺激是进行大脑功能区定位、癫痫病灶识别以及治疗性神经调控的关键技术。然而,在当前的临床实践中,为了获取更高质量的脑电信号,往往不得不承受更高程度的手术创伤,两者之间始终存在难以调和的矛盾。头皮脑电图(EEG)虽然安全性高且易于临床普及,但受限于颅骨对信号的衰减作用以及容积传导效应,其空间分辨率相对较低,
且对大脑深部或脑沟内神经活动的敏感性明显不足。癫痫领域的侵入性颅内脑电图评估正是这一技术局限性的典型体现。在非病灶性癫痫、深部癫痫发作,或涉及复杂脑沟及内侧网络的病例中,头皮脑电图往往无法精确勾画出手术靶点,因此必须依赖颅内监测。硬膜下电极网格能够提供高密度的皮层标测,但通常需要进行开颅手术,并伴随着与手术相关的并发症风险。
这类设备在需要大范围探查皮层区域,或必须精准界定重要功能区时极具价值。通过直接从皮层表面采集信号,电极网格可以捕捉跨脑回的空间梯度变化,并支持基于电刺激的功能定位;然而,其监测范围受限于开颅手术的边界,且难以触达大脑深部或内侧结构。
立体定向脑电图(SEEG)通过立体定向技术植入深部电极,对呈三维分布的神经网络进行采样,从而部分克服了上述局限性。SEEG能够在最大程度减少脑表面暴露的前提下,对深部、双侧,或位于脑沟及内侧的癫痫起始区进行探查。它非常适合基于临床假设的病灶定位及网络层面的分析,但该技术要求极其严密的穿刺路径规划,并且将出血作为首要的手术风险。除了病灶定位,颅内记录还可以检测到诸如高频振荡等生物标志物,这些标志物已被证实与致痫组织密切相关。
类似的限制同样存在于深部脑刺激(DBS),以及旨在为重度瘫痪患者恢复沟通或运动控制能力的侵入性脑机接口(BCI)领域。横跨癫痫、运动障碍和瘫痪等多个领域,一个反复出现的挑战始终存在。振幅最高的神经记录和最精准的局灶性刺激,通常都需要付出最高程度侵入性手术的代价。
因此,临床上仍然迫切需要一种近脑接口,它既能提供优于头皮脑电图的信号质量,又能显著降低基于开颅手术的皮层脑电图(ECoG)或多路径SEEG所带来的手术并发症和技术门槛。血管内途径之所以备受瞩目,正是因为它们巧妙利用了神经介入医生日常操作中已十分熟悉的自然解剖通道,为触达皮层及皮层下靶点提供了一种全新的范式。
血管内神经接口旨在通过利用神经介入领域已经成熟的导管入路和设备输送体系,在手术侵入性与信号振幅之间找到一个实用的平衡点。从临床转化的视角来看,这一途径将技术的核心考量从“能否记录到脑电信号?”转化为“能否安全地植入并管理一种血管内器械?”。因此,设备的可输送性、物理形态、致血栓风险、内皮化过程、血管通畅性、影像学兼容性,以及植入后的长期随访监测,自然成为了决定该技术可行性与安全性的核心要素。
大脑的静脉解剖结构对该技术尤为有利:硬脑膜静脉窦和皮层浅静脉的走行紧贴大脑皮层,这不仅缩短了记录距离,同时静脉系统较低的血流搏动也为搭载电极的设备提供了相对稳定的管腔容纳空间。然而,个体间的血管解剖差异,包括血管口径、迂曲程度以及血管壁的顺应性,会直接影响设备能否稳固贴附于血管壁。此外,一旦发生静脉狭窄或血栓,其引发的临床后果严重程度在很大程度上取决于患者自身的静脉引流模式及侧支代偿能力。
纵观各类血管内脑机接口策略,这些平台不可避免地继承了传统神经血管植入物所面临的临床管理挑战:包括抗栓治疗方案的制定、血栓栓塞风险的防范、长期血管通畅性的维持,以及在出现设备并发症时可能面临的翻修或取出难题。因此,要对这些系统进行真正具有临床意义的评估,就必须将神经信号性能与植入物长期管理及患者安全的现实考量进行综合权衡。
血管内神经接口的历史发展主要围绕三个核心目标展开:(i) 实现贴近大脑的高带宽信号采样;(ii) 在动态的血管环境中保持电极位置的稳定性;(iii) 确保长期的生物相容性,且不产生不可接受的血栓栓塞风险。
早期的血管内“导线记录”证实了该途径的可行性,但也暴露了波形干扰(伪影)严重以及游离电极在搏动性血管中不稳定的弊端。
在20世纪90年代至21世纪初,相关研究愈发关注具有临床意义的监测靶点,并将记录时间延伸到了血管造影室之外。在癫痫领域,经静脉入路展现了重要影响力:例如通过双侧经颈静脉放置电极的“海绵窦脑电图”,成功检测到了明确的发作间期癫痫样放电(IEDs),并捕捉到了符合颞叶内侧起始特征的发作期模式。这些早期研究证实了静脉贴近性能够提高深部癫痫活动的检出率,同时也凸显了伪影干扰和静脉解剖变异带来的挑战。
技术发展的一个关键转折点是从单触点导线向多通道导管系统的过渡。多通道导管使得在临床流程中(如颈内动脉异戊巴比妥试验,即Wada试验)同时进行多部位血管内脑电记录成为可能,尽管动脉搏动伪影和管壁接触不稳依然是难题。随后的临床前研究进一步推动了多电极静脉记录的发展,并通过在受控条件下将血管内信号与硬膜外或硬膜下记录进行对比,初步确立了性能基准。这些研究明确了血管内记录所能达到的分辨率及其局限性。
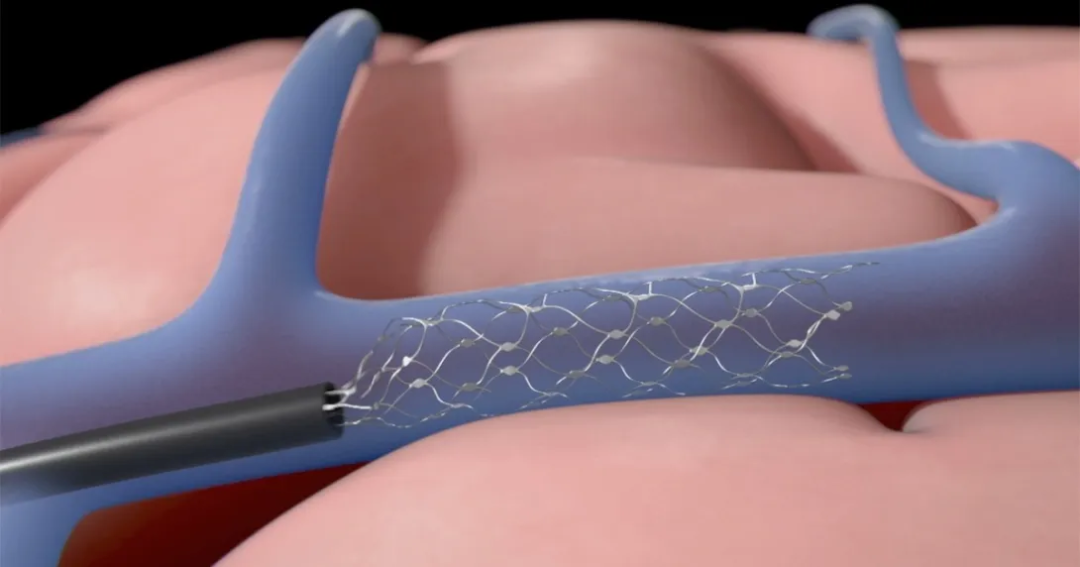
实现长期稳定性的重大概念飞跃是将电极集成到血管支架(如支架或脚手架式阵列)中。这种设计利用支架的自我扩张特性来维持与血管壁的稳定贴附,并有望通过内皮化过程促进生物学整合。这种设计策略对神经介入医生而言非常熟悉,它将长期的神经接口问题转化为了血管植入物的设计问题。
现代血管内神经接口因此涵盖了三大体系:
(i) 用于诊断性记录的临时性导管电极系统;
(ii) 用于静脉皮层脑电图(vECOG)的慢性支架电极阵列;
(iii) 旨在通过超柔性探针、无引线遥测及无线供电架构来提高分辨率并减轻导线负担的新兴系统。

本综述主要聚焦于已进入早期人体应用或处于相对后期转化阶段的血管内神经接口平台。为了全面评估这些平台,我们采用了一个基于神经介入视角的四维框架:预期临床用途、神经信号性能、手术可行性以及植入物管理。这具体涵盖了设备是用于短期诊断还是慢性植入、用于信号记录还是神经刺激,以及介入路径设计和与之相关的现实挑战——例如血栓栓塞风险、抗栓策略、血管通畅性监测、感染防范以及设备的翻修或拔除。
目前具有代表性的两大前沿平台如下:
-
Stentrode 支架电极阵列:用于慢性脑机接口(BCI) 基于支架电极阵列的血管内脑机接口旨在通过神经介入途径,在不开颅的前提下实现稳定且贴近皮层的长期信号记录。与短暂的导管记录不同,该设备通过支架样结构固定在邻近感觉运动皮层的静脉系统内(通常是上矢状窦),从而实现长期的“静脉皮层脑电图(vECOG)”监测。
其向人体的转化过程遵循了直观的临床逻辑。首次人体功能性应用及随后的 SWITCH 首批人体试验确立了其早期的安全性与可行性:血管内植入的接口成功支持了重度瘫痪患者对数字设备的意念控制,且在12个月的随访期内,未观察到设备移位、靶静脉闭塞或严重的设备相关不良事件。随着临床经验的积累,研究已开始明确 vECoG 在实际应用中可提取的神经特征,例如解析与运动意图相关的信号调制,以及对眼球扫视运动进行分类解码。
此类慢性植入物的长期转化高度依赖于血管生物学反应和抗栓策略的制定。大动物模型显示,设备会逐渐被血管壁的内皮组织包绕融合,尽管静脉窦会发生重塑,但仍能保持血流通常。在现有的人体试验中,患者接受了严格的抗血小板治疗及影像学随访(例如 SWITCH 研究中要求术前两周启动双抗,术后维持三个月,随后长期服用阿司匹林),这为慢性静脉接口的血栓风险管理提供了目前的参考基准。
-
EP-01:兼容微导管的多位点血管内脑电图系统 EP-01(由日本 Epsilon Medical 研发)瞄准了与慢性 BCI 截然不同的临床需求:以微创方式获取近颅内脑电信号,用于癫痫的术前评估。其核心工作流是通过标准的神经介入路径,将多根记录电极精准部署在颅内的多个静脉位点(通常为双侧),最长可维持约2周的持续脑电记录,并在达成诊断目标后将系统完整拔除。
这种“临时但具有一定时长”的监测范式,需要采用与常规癫痫评估流程相匹配的临床终点来衡量其价值,包括发作间期癫痫样放电(IED)的检出率以及侧向化诊断的准确性。临床前研究证实了其优于传统无创手段的潜力:血管内脑电图能够捕捉到硬膜下电极已探测到、但头皮脑电图却遗漏的局灶性癫痫样放电。

在人体转化方面,研究证实了其在受试者中记录到了比头皮脑电图振幅更高的 IED,且操作期间未发生出血或血栓并发症。目前,迈向常规临床应用的关键一步,是从单臂可行性观察过渡到具有对比终点的正式临床研究。例如正在开展的多中心前瞻性 EPSILON IE 试验,正是以“血管内脑电图与传统开颅颅内脑电图在侧向化诊断上的一致性”作为核心判定指标。此外,由于该系统需要将导线引出体外连接传统脑电设备,长达两周留置期内的感染预防和防血栓管理(如持续的肝素盐水冲洗),是其在临床操作层面必须妥善应对的挑战。


临床解释、报告标准与具有临床价值的终点
血管内神经接口的普及将取决于它们能否像成熟的血管植入物一样被安全输送和管理,并表现出可预测的性能。关键要求包括可重复的精准放置、可接受的手术负担、持久的血管通畅性,以及与常规临床路径相兼容的监测计划。目前的核心不确定性在于长期的植入物生物学反应和抗栓方案的权衡。慢性支架类接口可能需要抗血小板治疗,这带来了如何在血栓风险与出血风险之间取得平衡的现实问题,特别是考虑到患者未来可能需要接受其他介入或外科手术。
临床报告应当详细说明抗栓方案,并在条件允许时提供血管影像学随访依据。必须尽早明确设备随访规范和失效模式,最低限度的报告要素应包括:必要时的影像学随访、信号稳定性指标、通道丢失率,以及设备移位、断裂或穿刺部位并发症等不良事件。对于新兴设备,即使极少需要拔除,血管内翻修或取出的可行性也会直接影响医患对风险的接受度及最终的适应症选择。
设备的可拔除性和感染风险是影响技术普及的重要考量,但不同技术平台之间存在显著差异。慢性完全植入系统与短期体外引出系统在感染风险图谱、设备管理要求和拔除策略上存在本质区别。Stentrode 在设计上并非作为可常规拔除的接口,而 EP-01 的初衷即为满足短期放置和最终完全移除的诊断需求。
当前影响疗效证据客观解读的一个主要障碍是信号报告标准的极其不统一。记录质量受血管运动、电极与组织间距、静脉解剖变异、参考电极设置及环境伪影等多重复杂因素影响。未来的研究应向统一的最低基准迈进,包括规范的脑电信号采集要求、预先设定的伪影处理原则、一致的参考电极设置,以及明确的不良事件报告机制。
最重要的是,临床试验设定的终点应该与实际医疗工作流中具有指导意义的决策相挂钩,而不仅仅是停留在证明“能够探测到脑电信号”的层面。在癫痫领域,核心问题在于血管内记录能否以与传统开颅颅内脑电监测相一致的方式,切实改善致痫灶的侧向化或精确定位诊断。
EPSILON IE 多中心试验正是这种具有临床转化导向评估理念的前瞻性框架。对于意图恢复运动或交流能力的辅助性脑机接口,评价终点应聚焦于持续且稳定的功能解码表现,并透明地报告长期信号衰减、通道丢失以及设备初始输送失败的情况。总体而言,现有证据支持了静脉内记录技术的初步可行性,包括 Stentrode 等慢性植入接口的早期人体试验,以及 EP-01 在癫痫术前评估流程中的短期多位点诊断性应用。但目前的循证依据尚未建立起标准化的抗栓策略、广泛的解剖适用性、常规拔除及翻修路径,也无法证实其全面优于已确立的传统有创颅内脑电手段。
新兴与临床前发展方向
与神经记录相比,血管内神经刺激仍处于更早期的转化阶段。虽然前期建模、解剖学分析和近期的大动物实验表明,在特定的静脉几何及电学条件下对选定靶点进行血管内深部脑刺激(DBS)具备初步可行性。但刺激功能面临着更为严苛的物理及生物学约束,如电荷注入安全极限、电极极化效应、脑组织对重复脉冲的耐受性,以及对获取坚实长期血管通畅性数据的高门槛需求。
目前在工程探索端有两种策略有望进一步拓展血管内神经接口的能力边界:提高空间分辨率和减轻导线解剖负担。例如,近期有研究展示了一种超柔性血管内阵列能够在动物模型中记录皮层单神经元层面的尖峰放电,展示了突破传统静脉记录空间限制的潜力,但也暴露出血管壁厚度干扰和柔性器件在复杂血管内壁输送力学机制等深水区转化瓶颈。同时,无引线供电和无线遥测技术正在被研发,以此消除经颈静脉长导线这一慢性系统中的潜在机械故障和感染风险点。
尽管 EP-01 目前的产品定位为短期诊断性监测,但其多位点、微导管兼容的系统特性引发了业界更长远的探讨:更为广泛且分布式的静脉网络采样是否足以支持未来慢性脑机接口的复杂意图解码范式?这一设想仍属推测,必须通过预设的功能学验证终点和透明的失效归因报告来严谨求证。
鉴于人群中皮层上静脉引流解剖存在着极大的异质性,这种化整为零的多靶点策略可能比依赖单一大型支架植入物提供更大的解剖学适应空间,这也印证了血管内脑机接口的植入必须高度依赖个性化术前影像学规划的共识。此外,在动脉瘤性蛛网膜下腔出血等神经重症场景中,EP-01 的设计允许其在硬膜静脉窦和皮层引流静脉内进行灵活的床旁部署,为探测非惊厥性癫痫发作及重症脑生理监测提供了一种极具弹性的微创替代方案。
血管内神经接口正逐渐成为连接无创头皮电生理技术与传统开颅直视植入物之间的一座重要过渡桥梁。现有平台的推进证明,无论是用于解决近期的诊断痛点,还是着眼于长期的残疾辅助设备控制,均可从颅内静脉靶点获取具有实际转化价值的神经信号。
该技术路径最终能否真正走向大规模常规临床应用,取决于行业能否建立标准化的临床操作与报告规范、设定真正具有临床指导意义的评价终点,并通过严谨的前瞻性队列研究,验证其在克服个体解剖变异及保障设备与血管系统长期生物相容性方面的可靠性。妥善解决上述挑战后,血管内途径将确立为神经调控与脑机接口领域一种极具实用价值的补充工具,而非对既有传统监测及手术手段的完全替代。










